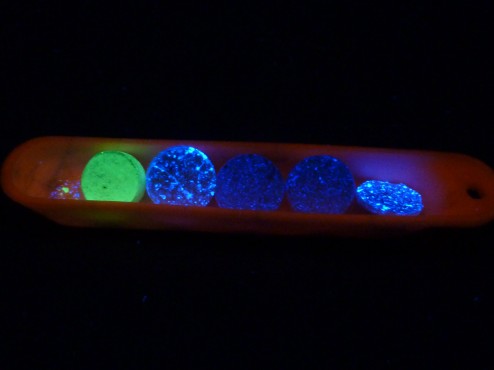
Différents phosphorescent après frittage .Cette synthèse a été mise au point spécifiquement pour Chimie science magique et a été publiée dans the journal of Chemical Education. Synthétisés pour le première fois en chimie magique par synthèse micro-ondeSynthèse d’un phosphorescent
Un élément dit luminescent comporte la propriété d’absorber de l’énergie lumineuse (lumière d’excitation) et de la libérer ensuite sous forme de lumière (lumière d’émission). Lorsque l’énergie constituant le photon est absorbée, la molécule se trouve généralement dans un état excité. Le retour à l’état fondamental peut alors se faire soit par fluorescence, soit par phosphorescence. La fluorescence est l’émission rapide d’un photon précédée par l’excitation d’une molécule par absorption d’un photon. La phosphorescence est le phénomène observé lorsqu’une matière continue à émettre de la lumière après avoir été éclairée dans une certaine longueur d’onde. Le phénomène de phosphorescence est dû à une réaction : il s’agit de la perte d’énergie par des électrons qui ont été excités et qui retournent ensuite à des niveaux d’énergie plus bas. Des matières phosphorescentes comme les aluminates de terres rares sont utilisées dans la plupart des matériaux phosphorescent nous entourant.
Dans le cadre de l’UE «chimie magique» nous synthétisons un phosphorescent dit longue durée fait à partir d’aluminate de strontium dopé à l’europium et au dysprosium.
Nouveaux phosphorescents
Il existe plusieurs phosphorescents de différentes couleurs comme les phosphorescents bleus, verts, violets, rouges, etc… Ce sont
des éléments capables de continuer à émettre de la lumière après avoir été éclairée à une certaine longueur d’onde. En effet, le phénomène de phosphorescence est dû à une suite de pertes d’énergie des électrons au préalablement excités qui retournent lentement à des niveaux d’énergie plus bas.
Mais il ne faut pas confondre phosphorescence et fluorescence, car ce sont deux notions bien distinctes! Ainsi le fluorescent émet un photon très rapidement tandis que le phosphorescent, lui, est plus lent.
En chimie magique on inaugure de nouvelles techniques, c’est donc une synthèse faite au micro-onde que nous avons utilisé afin de faire un phosphorescent bleu dopés à l’europium dans une matrice BaMgAl10O17.
Équation de la réaction:
Ba(NO3)2 + Mg(NO3)2 + 10Al(NO3)2 + Eu(NO3)2 + 14CO(NH2)2 => BaMgAl10O17 + Eu(II) + 37,5CO2 + 14(NH2)2
Le protocole:
– diluer avec le minimum d’eau dans un bécher:
- 278 mg de nitrate de baryum
- 273 mg de nitrate de magnésium
- 4 g de nitrate d’aluminium
- 20 mg de nitrate d’europium
– une fois les nitrates bien dissous on met 7,3 g d’urée.
– On met ensuite cette solution au micro-onde à 1000W pendant
3 à 5 minutes ou jusqu’à explosion.
– le précurseur est ensuite broyer au mortier et lavé sur büchner
– sécher la poudre sur papier filtre
Pour montrer l’efficacité de ce phosphorescent, on expose notre poudre au UV d’une longueur d’onde de 380nm. On retrouve un phosphorescent de couleur bleu qui persiste après l’exposition au UV.
Variante :
Synthèse d’un phosphorescent jaune et d’un phosphorescent vert :
- 3,376 g de nitrate d’aluminium * 3,376 g de nitrate d’aluminium
- 1,026 g de nitrate de strontium * 1,144 g de nitrate de calcium
- 22 mg de nitrate de europium * 22 mg de nitrate de europium
- 46 mg de nitrate de dysprosium * 46 mg de nitrate de dysprosium
- 7,6 g d’urée * 7,6 g d’urée
On a donc pu observer qu’en remplaçant le strontium par du calcium on obtenait des variantes dans la couleur du phosphorescent. De multitudes de synthèses sont encore possibles, à vous de jouer !!!!
Auteurs:
- FAYOLLE laura
- LEBLANC Martin
- TARIF Laura




